Generalmente la terapia d’elezione per la malattia da reflusso gastroesofageo (MRGE) prevede l’utilizzo degli inibitori di pompa protonica (IPP). Questi farmaci, infatti, abbattono la secrezione di acido gastrico, limitando così l’esposizione dell’esofago al reflusso acido dello stomaco. L’utilizzo degli IPP si è dimostrato efficace nella cura dell’esofagite, riducendo l’infiammazione dell’esofago e accelerando la cicatrizzazione delle sue lesioni. Tuttavia, in alcuni pazienti, l’interruzione della terapia può portare alla ricomparsa dei sintomi, costringendoli ad un’utilizzo continuativo del gastroprotettore, non sempre efficace e non esente da effetti collaterali. Inoltre una significativa percentuale dei pazienti, stimata tra il 20% e il 40%, non risponde alla terapia con IPP. In questi casi è prevista l’aumento dei dosaggi del gastroprotettore o l’aggiunta di farmaci add-on, sebbene i risultati non sempre migliorino. In questi casi i pazienti sono soliti valutare l’opzione chirurgica alla ricerca di una cura definitiva per il reflusso gastroesofageo.
Chirurgia anti-reflusso: è la cura definitiva?
I pazienti refrattari alla terapia con IPP o quelli che ne diventano dipendenti per la gestione dei sintomi considerano l’intervento chirurgico come una possibile cura definitiva per il reflusso gastroesofageo. Ma è effettivamente così?
Innanzitutto l’operazione chirurgica per il reflusso gastroesofageo è la fundoplicatio sec Nissen, cioè la piegatura del fondo gastrico secondo la tecnica di Nissen, il chirurgo che l’ha creata. L’intervento prevede di ripiegare il fondo gastrico attorno all’esofago, così da creare due tasche che cingono lo sfintere esofageo (si veda fig.1). Quando il reflusso spinge il contenuto gastrico verso l’alto, le tasche si gonfiano, come fossero un paracadute. La dilatazione delle tasche comprime l’esofago, chiudendolo e impendendo la risalita del contenuto gastrico.
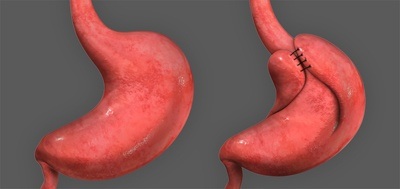
Fig. 1 – Chirurgia anti-reflusso – Fundoplicatio secondo Nissen
L’intervento ha una scarsa invasività, essendo eseguito in laparoscopia. La principale complicanza è la disfagia, cioè la difficoltà di deglutizione, che generalmente si risolve dopo alcuni giorni dall’intervento ma, talvolta, potrebbe protrarsi nel tempo.
La chirurgia anti-reflusso di Nissen ha dimostrato un’efficacia maggiore rispetto alla terapia farmacologica prevista per i casi che non rispondono agli IPP. In uno studio randomizzato pubblicato sul The New England Journal of Medicine, infatti, l’operazione chirurgica è risultata più efficace rispetto all’utilizzo combinato dell’omeprazolo e del baclofen, associati in alcuni casi anche all’antidepressivo desipramina. In particolare l’intervento ha ridotto significativamente i sintomi del reflusso nel 67% dei casi, rispetto al solo 28% di quelli che invece seguivano la terapia farmacologica[1].
La chirurgia antireflusso è quindi maggiormente efficace della terapia farmacologica nei pazienti refrattari agli IPP. Tuttavia circa il 30% dei pazienti sottoposti all’intervento non ha avuto alcun beneficio. Soprattutto, in una quota non trascurabile di pazienti, stimata attorno al 20%, i sintomi del reflusso si ripresentano nel tempo, costringendo i pazienti a riprendere la terapia farmacologica o a una nuova operazione. L’intervento di fundoplicatio secondo Nissen non sempre, quindi, è una cura definitiva per il reflusso gastroesofageo.
Nuove cure per il reflusso gastroesfageo
Fundoplicazione transorale senza incisione
La fundoplicazione transorale senza incisione(o transoral incisionless fundoplication – TIF) è una tecnica che ricostruisce lo sfintere esofageo per via endoscopica (in gastroscopia) e senza incisioni. Essa prevede l’utilizzo di un endoscopio attraverso il quale si vanno ad ancorare i tessuti dello sfintere esofageo, in modo simile alla fundoplicazione di Nissen, ma senza incisioni chirurgiche. I particolari endoscopi utilizzati, infatti, permettono di ricompattare i tessuti esofagei, attraverso l’applicazione di semplici punti di sutura. Si ripristina, così, il tono dello sfintere esofageo, limitando la risalita di acido dallo stomaco verso l’esofago.
Generalmente la fundoplicazione transorale senza incisione viene eseguita con il dispositivo Esophyx (si veda fig. 2) o con la suturatrice ad ultrasuoni MUSE (si veda fig. 3). Altre metodiche per effettuare la TIF sono lo strumento Endocinch e il dispositivo GerdX.
Fig. 2 – Procedura di fundoplicazione transorale senza incisione effettuata con endoscopio Esophyx.
Fig. 3 – Procedura di fundoplicazione transorale senza incisione effettuata con endoscopio MUSE
Le procedure TIF hanno dimostrato una significativa riduzione dei sintomi del reflusso gastroesofageo in soggetti refrattari agli IPP. In uno studio che ha seguito i pazienti per i 5 anni successivi la TIF con Esophyx, il miglioramento dei sintomi è perdurato nell’82% dei pazienti a distanza di un anno e nell’80% a distanza di 5 anni. Inoltre a 5 anni solo il 30% dei pazienti continuava ad assumere gli inibitori di pompa[2]. In uno studio prospettico multicentrico sulla TIF eseguita con MUSE l’83,8% (31/37) e il 69,4% (25/36) dei pazienti sono rimasti senza prendere il gastroprotettore, rispettivamente, per 6 mesi e 4 anni[3]
I risultati positivi mostrati dalla TIF la pongono come una possibile alternativa, meno invasiva e con un’efficacia simile, alla fundoplicazione di Nissen. Tuttavia nel lungo termine i punti di sutura del tessuto esofageo possono cedere, riportando lo sfintere esofageo alla sua configurazione iniziale.
Neurostimolazione esofagea
La neurostimolazione esofagea prevede l’impianto sottopelle di un piccolo elettrostimolatore, commercializzato con il nome Endostim. Il dispositivo ha due elettrodi collegati allo sfintere esofageo, che riceve corrente elettrica a bassa frequenza. L’idea alla base di questo approccio è che la stimolazione elettrica dello sfintere sia in grado di ripristinare il suo corretto funzionamento, sostenendone la chiusura dopo il passaggio del cibo.
La procedura è minimamente invasiva; gli elettrodi sono infatti collegati allo sfintere in laparoscopia. L’intervento, inoltre, è reversibile. La rimozione del dispositivo o il suo semplice spegnimento, infatti, ne interrompono l’effetto sull’esofago.
Fig. 3 – Neurostimolazione esofagea Endostim – Fonte: Two -year results of Lower Esophageal Sphincter Stimulation for the Treatment of Gastroesophageal Reflux Disease
La neurostimolazione esofagea riduce i sintomi del reflusso gastroesofageo. In uno studio eseguito su pazienti parzialmente rispondenti agli IPP prima e dopo l’applicazione del dispositivo, l’elettrostimolazione ha ridotto l’esposizione dell’esofago all’acido gastrico, limitando i sintomi del rigurgito acido, senza una delle complicanze più comuni agli altri interventi, la disfagia.[4]. Un risultato, quest’ultimo, che evidenzia il potenziale terapeutico di quest’approccio per la cura del reflusso. Tuttavia l’esatta efficacia della neurostimolazione è ancora incerta, ma i risultati preliminari positivi e le minori complicanze rispetto agli interventi di fundoplicazione, suggeriscono ulteriori approfondimenti.
Trattamento a radiofrequenza
Il trattamento a radiofrequenza con tecnologia “Stretta” si esegue per via endoscopica (gastroscopia) attraverso l’applicazione di elettrodi ad ago nell’esofago distale. In particolare essa prevede l’introduzione nello sfintere gastroesofageo di un palloncino che, gonfiandosi, spinge gli elettrodi ad ago sulla mucosa dello sfintere. L’emissione di radiofrequenze dagli aghi, a sua volta, causa l’ablazione della mucosa esofagea. La mucosa viene quindi “bruciata” e, in risposta, sviluppa un tessuto fibrotico insensibile agli stimoli dolorosi. In tal modo il contatto della mucosa esofagea con l’acido gastrico non dovrebbe più scatenare la percezione di dolore o bruciore di stomaco. Il trattamento con le radiofrequenze è quindi meramente sintomatico.
Inoltre il trattamento a radiofrequenza dovrebbe anche aumentare il tono dello sfintere esofageo inferiore (LES), stimolando la muscolatura liscia del LES (si veda fig. 4). Studi meccanicistici, infatti, mostrano che Stretta stimola la crescita della muscolatura liscia e diminuisce la compliance dei tessuti, consentendo un minor numero di episodi di reflusso e portando a un significativo miglioramento dei sintomi della MRGE. Tuttavia una meta-analisi ha mostrato come il suo utilizzo non produca effetti significativi nella riduzione dei sintomi del reflusso gastroesofageo[5], raccomandando lo svolgimento di studi più rigorosi e ampi.
Potenziamento magnetico dello sfintere esofageo
Il potenziamento magnetico dello sfintere esofageo prevede l’applicazione per via endoscopica di una collarino magnetico attorno allo sfintere esofageo. L’idea è che l’attrazione delle biglie magnetiche che lo compongono sia in grado di sostenere la chiusura dello sfintere, impendendo la risalita di contenuto gastrico.
Musectomia anti-reflusso
La musectomia anti-reflusso è una tecnica endoscopica che prevede la resezione della mucosa dello stomaco in prossimità dello sfintere esofageo. L’idea alla base di questo approccio è che il processo di guarigione della mucosa, conseguente la sua resezione, porti alla formazione di tessuto cicatriziale e al conseguente restringimento dello sfintere esofageo. In tal modo il volume del reflusso gastrico sarebbe limitato dalla minore ampiezza dello sfintere esofageo.
In uno studio condotto in Giapppone su 109 pazienti refrattari alla terapia con IPP, la musectomia ha migliorato significativamente i sintomi del reflusso nel lungo termine e, circa la metà dei pazienti, è riuscita ad interrompere la terapia con IPP[6]. I risultati, seppur promettenti, devono però essere ulteriormente approfonditi.
Conclusioni
Nei pazienti che non rispondono alla terapia con IPP o in quelli che non vogliono prendere i farmaci in modo continuativo è possibile valutare l’opzione chirurgica che, sebbene non rappresenti una cura definitiva per il reflusso gastroesofageo per la totalità dei pazienti, può in una buona parte di loro produrre risultati duraturi, limitando i sintomi senza ricorrere ai farmaci. Ciascuna modalità d’intervento ha vantaggi e svantaggi che devono essere valutati approfonditamente tenendo conto delle specificità del paziente. Vale la pena ricordare, soprattutto, che un fattore chiave per il successo dell’intervento è la competenza dell’operatore che esegue la procedura. Per questa ragione è raccomandabile rivolgersi a centri d’eccellenza con una lunga e consolidata esperienza.
Bibliografia
- Rodriguez, Leonardo & Rodriguez, Patricia & Gómez, Beatriz & Ayala, Juan & Oxenberg, Daniel & Perez-Castilla, Alberto & Neto, Manoel & Soffer, Edy & Boscardin, John & Crowell, Michael. (2014). Two -year results of Lower Esophageal Sphincter Stimulation for the Treatment of Gastroesophageal Reflux Disease. Surgery. 157.
- Trad KS, Barnes WE, Prevou ER, Simoni G, Steffen JA, Shughoury AB, Raza M, Heise JA, Fox MA, Mavrelis PG. The TEMPO Trial at 5 Years: Transoral Fundoplication (TIF 2.0) Is Safe, Durable, and Cost-effective. Surg Innov. 2018 Apr;25(2):149-157.
- Kim HJ, Kwon CI, Kessler WR, Selzer DJ, McNulty G, Bapaye A, Bonavina L, Lehman GA. Long-term follow-up results of endoscopic treatment of gastroesophageal reflux disease with the MUSE™ endoscopic stapling device. Surg Endosc. 2016 Aug;30(8):3402-8.
- Kappelle WF, Bredenoord AJ, Conchillo JM, Ruurda JP, Bouvy ND, van Berge Henegouwen MI, Chiu PW, Booth M, Hani A, Reddy DN, Bogte A, Smout AJ, Wu JC, Escalona A, Valdovinos MA, Torres-Villalobos G, Siersema PD. Electrical stimulation therapy of the lower oesophageal sphincter for refractory gastro-oesophageal reflux disease – interim results of an international multicentre trial. Aliment Pharmacol Ther. 2015 Sep;42(5):614-25.
- Lipka S, Kumar A, Richter JE. No evidence for efficacy of radiofrequency ablation for treatment of gastroesophageal reflux disease: a systematic review and meta-analysis. Clin Gastroenterol Hepatol. 2015 Jun;13(6):1058-67.e1.
- Sumi K, Inoue H, Kobayashi Y, Iwaya Y, Abad MRA, Fujiyoshi Y, Shimamura Y, Ikeda H, Onimaru M. Endoscopic treatment of proton pump inhibitor-refractory gastroesophageal reflux disease with anti-reflux mucosectomy: Experience of 109 cases. Dig Endosc. 2021 Mar;33(3):347-354.